每日經濟新聞 2022-07-25 23:56:40
◎真實生物的阿茲夫定片增加治療新冠病毒肺炎適應癥注冊申請。可用于治療普通型新型冠狀病毒肺炎成年患者。此前,它已經是國內首個擁有自主知識產權的抗艾滋病毒口服核苷類藥物。
◎阿茲夫定還涉及三家A股上市公司,華潤雙鶴、奧翔藥業、新華制藥。它們與真實生物就阿茲夫定的生產簽訂了《戰略合作協議》或《委托加工生產框架協議》。
每經記者 林姿辰 每經編輯 文多
國產新冠口服藥物終于來了。
國家藥品監督管理局(NMPA)官網消息,今日(7月25日),國家藥監局根據《藥品管理法》相關規定,按照藥品特別審批程序,進行應急審評審批,附條件批準河南真實生物科技有限公司(簡稱“真實生物”)阿茲夫定片增加治療新冠病毒肺炎適應癥注冊申請。
這意味著,真實生物的阿茲夫定片成為國內首款自主研發的口服小分子新冠治療藥物。
同日,在全國藥品監督管理工作電視電話會議上,國家藥監局方面明確提出“加快新冠病毒治療藥物研發上市速度”。
據西南證券7月研報,目前除真實生物的阿茲夫定獲批外,國產新冠口服藥處于研發后期的藥物還包括君實生物(SH688180,股價64.35元,市值587億元)的VV116以及開拓藥業(HK09939,股價16.60港元,市值64億港元)的普克魯胺等。
此外,有10余款國產新冠口服藥處于研發早期,不過,這些藥物較少針對重癥患者人群。
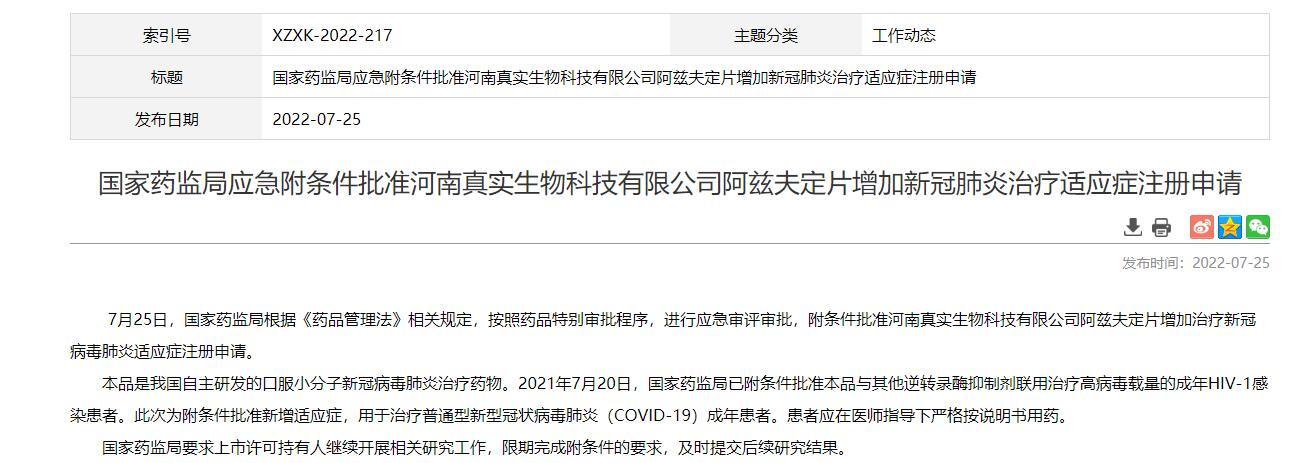
圖片來源:網頁截圖
去年7月20日,阿茲夫定片獲國家藥監局附條件批準,可與其他逆轉錄酶抑制劑聯用治療高病毒載量的成年HIV-1感染患者,成為國內首個擁有自主知識產權的抗艾滋病毒口服核苷類藥物。
此次該藥物再被附條件批準新增適應癥,可用于治療普通型新型冠狀病毒肺炎(COVID-19)成年患者。國家藥監局官網顯示,患者應在醫師指導下嚴格按說明書用藥。國家藥監局還要求上市許可持有人繼續開展相關研究工作,限期完成附條件的要求,及時提交后續研究結果。
值得注意的是,真實生物的阿茲夫定曾在中國、巴西、俄羅斯開展針對新冠肺炎適應癥的Ⅲ期臨床試驗,7月15日公司宣布“Ⅲ期臨床試驗結果達到預期”。
阿茲夫定的價格優勢非常明顯。
據報道,作為艾滋病藥物,阿茲夫定的售價是25.86元/mg(片),每天5毫克使用量,一個療程35毫克,以艾滋病用藥定價,治療新冠單療程對應價格為900多元。據公司測算,原料藥到噸級可以降低至40萬一公斤,如對比原料藥同比例價格下降,單療程為240元。
對比輝瑞的Paxlovid在國內醫保2300元/盒的定價,阿茲夫定片的價格優勢明顯,若后期納入醫保,價格可能還會更低。
在A股市場,阿茲夫定涉及三家A股上市公司,它們與真實生物就阿茲夫定的生產簽訂了《戰略合作協議》或《委托加工生產框架協議》。
7月25日收盤,華潤雙鶴(SH600062,股價26.38元,市值275.21億元)、奧翔藥業(SH603229,股價48.00元,市值193億元)、新華制藥(SZ000756,股價23.67元,市值158.50億元)今年股價漲幅分別為102.01%、84.86%、111.53%。
盤后,復星醫藥(SH600196,股價48.94元,市值1254億元)發布公告,稱控股子公司復星醫藥產業與真實生物簽訂《戰略合作協議》,就推進雙方聯合開發并由復星醫藥產業獨家商業化阿茲夫定等事宜達成戰略合作。本次合作領域包括新冠病毒、艾滋病治療及預防領域。
25日下午,為了解更多阿茲夫定片的相關信息,記者通過微信聯系真實生物相關人士,對方暫未做出確切回復。
國內新冠口服藥的研發競速,不會因為阿茲夫定的上市放慢腳步。
西南證券7月研報顯示,截至7月3日,全球已有3款新冠口服藥上市,其中輝瑞的Paxlovid已在中國獲批上市;國內研發進度最快的分別為處于III期臨床的君實生物的VV116、真實生物的阿茲夫定和開拓藥業的普克魯胺。
截至7月3日,默沙東的莫奈拉韋已在國內提交新藥申請,君實生物/旺山旺水生物的VV116、海正藥業(SH600267,股價12.40元,市值148.57億元)的法維拉韋處于Ⅲ期臨床階段,先聲藥業(HK02096,股價8.77港元,市值232.13億港元)SIM0417針對輕中度新冠患者的研究處于Ⅱ/Ⅲ期臨床階段,針對暴露后預防的臨床研究申請已獲批。
此外,布局新冠口服藥物且處于早期研究階段的國內企業也不在少數,在研藥物主要以3CL蛋白酶抑制劑為主。
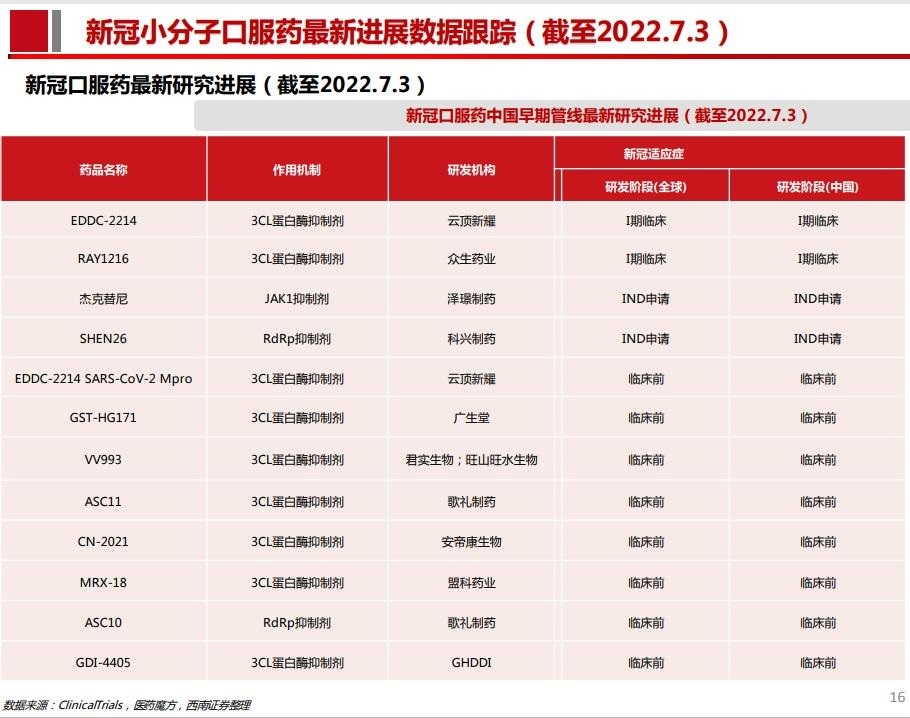
圖片來源:西南證券研報截圖拼接
記者注意到,處于研發早期的國內在研新冠藥物依舊眾多,其中國內企業澤璟制藥(SH688266,股價33.04元,市值79.30億元)的JAK1抑制劑杰克替尼針對重癥患者人群,截至7月3日處于臨床研究申請階段。
新聞鏈接:
阿茲夫定是“國產首款新冠口服藥”,區別于之前的“國產首款新冠特效藥”。
《國產首款新冠特效藥上市,口服藥市場擠壓下,抗體藥物利潤空間在哪里?》
封面圖片來源:攝圖網-500739443
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
