每日經(jīng)濟(jì)新聞 2022-08-20 08:19:28
每經(jīng)記者 文巧 每經(jīng)編輯 程鵬 蘭素英 易啟江
近日,美國(guó)食品藥品監(jiān)督管理局(FDA)批準(zhǔn)了藍(lán)鳥(niǎo)生物公司(BLUE,股價(jià)5.81美元,市值4.48億美元)的Zynteglo基因療法。
Zynteglo在美國(guó)的定價(jià)高達(dá) 280萬(wàn)美元(約合人民幣1908萬(wàn)元) ,超過(guò)諾華制藥(NVS,股價(jià)84.92美元,市值1853.62億美元)的脊髓性肌萎縮基因療法Zolgensma的定價(jià)210萬(wàn)美元,成為“史上最貴藥”。
該療法是一種一次性基因療法,也被稱為“beti-cel”,用于治療需要定期輸血的全部基因型β-地中海貧血。 這是FDA首次批準(zhǔn)針對(duì)β-地中海貧血患者的基因療法。彭博社稱,對(duì)于這類患者來(lái)說(shuō),該療法“改變了游戲規(guī)則”。在此之前, 針對(duì)該疾病唯一可用的治療方法是依靠患者親人進(jìn)行骨髓移植。
藍(lán)鳥(niǎo)生物是在基因療法的浪潮中誕生的,曾經(jīng),作為生物技術(shù)界的“寵兒”,華爾街投資者趨之若鶩,但如今,卻墜落至資金枯竭的邊緣。
在Zynteglo獲批上市這一消息的刺激下,藍(lán)鳥(niǎo)生物股價(jià)在當(dāng)?shù)貢r(shí)間8月17日上漲24%,次日盤(pán)前又一度大漲17%,不過(guò)18日收盤(pán),股價(jià)下跌14.31%,報(bào)收5.81美元/股。截至19日收盤(pán),股價(jià)小幅回彈,上漲2.75%,報(bào)收5.97美元。
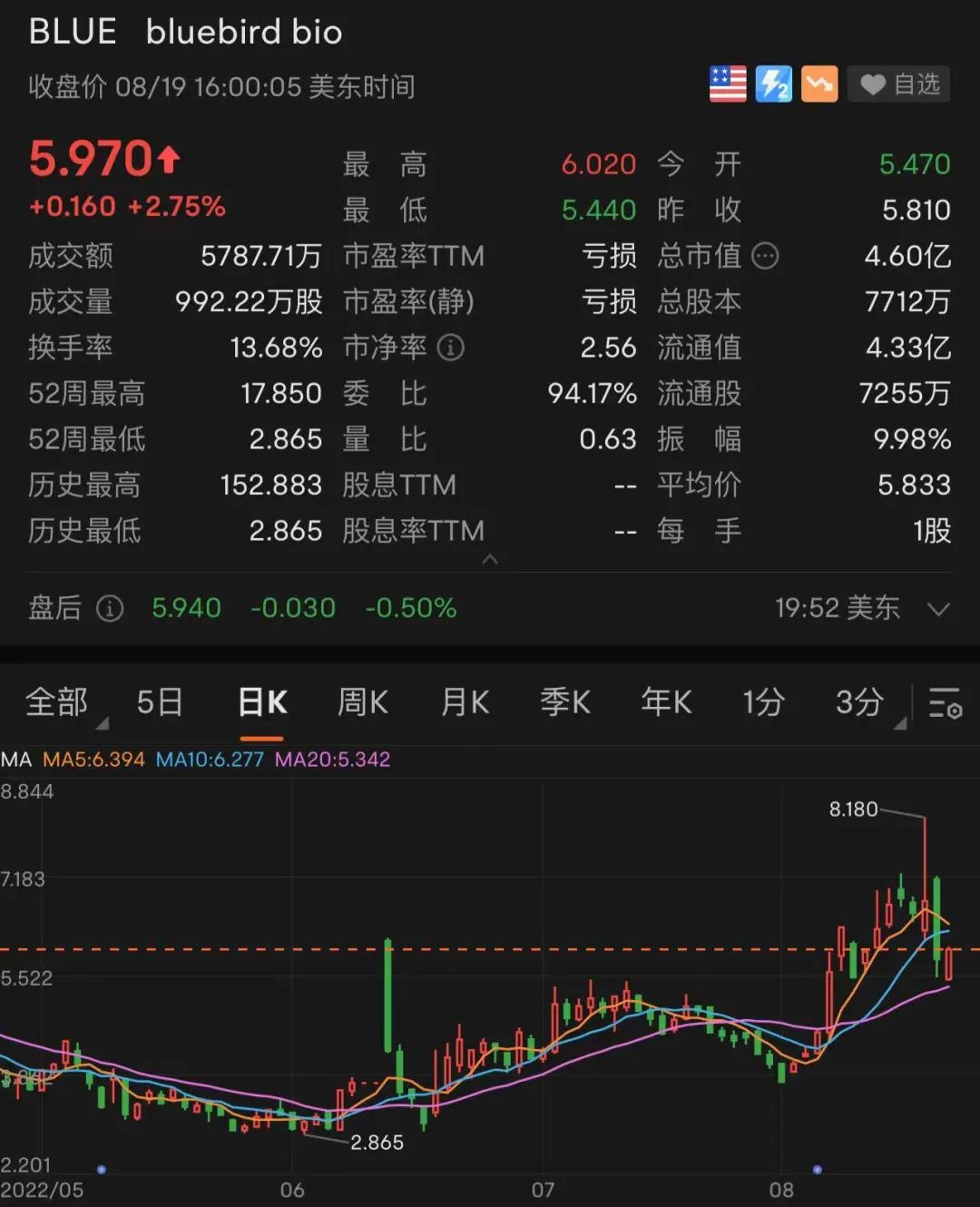
如今,憑借這款“史上最貴藥”,藍(lán)鳥(niǎo)生物能重新“騰飛”嗎?

圖片來(lái)源:攝圖網(wǎng)-400077451

“改變游戲規(guī)則”
今年6月份,F(xiàn)DA 顧問(wèn)小組一致投票支持批準(zhǔn)Zynteglo上市,稱這種治療的好處大于風(fēng)險(xiǎn)。據(jù)FDA,在后期試驗(yàn)中,接受Zynteglo基因療法的患者中有89%可以不必輸血,并且沒(méi)有任何明顯的安全問(wèn)題。
費(fèi)城兒童醫(yī)院血液科負(fù)責(zé)人Alexis Thompson 表示,盡管該基因療法并非對(duì)所有人都有效,但大多數(shù)患者中的生活都發(fā)生了巨大變化。費(fèi)城兒童醫(yī)院在臨床試驗(yàn)中就使用該療法進(jìn)行治療。Thompson透露,在此之前,需要輸血的β-地中海貧血患者每2~4個(gè)星期就要在醫(yī)院里待上4~6個(gè)小時(shí),有時(shí)甚至需要住院過(guò)夜。
據(jù)報(bào)道,β-地中海貧血是最常見(jiàn)的單基因疾病之一,由于編碼β珠蛋白的基因發(fā)生突變,患者體內(nèi)的血紅蛋白水平顯著下降甚至缺失,為了生存,患者不得不終身接受輸血治療。雖然輸血可以暫時(shí)緩解與嚴(yán)重貧血相關(guān)的癥狀,包括疲勞、虛弱和呼吸急促,但治標(biāo)不治本,并可能會(huì)出現(xiàn)因鐵過(guò)載和多器官損傷而導(dǎo)致的嚴(yán)重并發(fā)癥。
在過(guò)去十年中,美國(guó)輸血依賴型β地中海貧血患者的中位死亡年齡為37歲。
Zynteglo屬于一次性基因療法,通過(guò)慢病毒載體將β-珠蛋白基因?qū)氲交颊咦陨淼脑煅杉?xì)胞中,以生產(chǎn)正常的血紅蛋白,恢復(fù)紅細(xì)胞功能,從而顯著降低患者的輸血需求,在理想情況下,患者甚至不需要進(jìn)行輸血治療。
據(jù)彭博社報(bào)道,對(duì)于大部分時(shí)間需要依賴定期輸血的β-地中海貧血患者來(lái)說(shuō),這種療法“改變了游戲規(guī)則”。
不過(guò),F(xiàn)DA方面同時(shí)提示, 這種治療存在引發(fā)血癌的潛在風(fēng)險(xiǎn), 雖然在Zynteglo的研究中沒(méi)有看到任何病例,但接受Zynteglo治療的患者應(yīng)該對(duì)血液進(jìn)行至少15年的監(jiān)測(cè)。在Zynteglo給藥期間,還應(yīng)監(jiān)測(cè)患者的超敏反應(yīng)以及血小板減少和出血情況。

史上最貴
無(wú)療效可獲80%費(fèi)用報(bào)銷
據(jù)報(bào)道,在美國(guó),根據(jù)目前的護(hù)理標(biāo)準(zhǔn),輸血依賴型β地中海貧血患者的終生醫(yī)療費(fèi)用高達(dá)640萬(wàn)美元,每位患者每年的平均總醫(yī)療費(fèi)用是普通人群的23倍。據(jù)藍(lán)鳥(niǎo)生物估計(jì),美國(guó)約有1300~1500人患有β-地中海貧血疾病。
Zynteglo在美國(guó)的定價(jià)為280萬(wàn)美元,而在2019年5月獲批在歐盟上市時(shí),該療法的定價(jià)為157.5萬(wàn)歐元(按當(dāng)時(shí)的匯率,約合180萬(wàn)美元)的定價(jià)。盡管當(dāng)時(shí)在歐盟的價(jià)格相比現(xiàn)在還要便宜很多,但Zynteglo在歐洲的商業(yè)化進(jìn)程卻也面臨重重阻礙。2021年4月,藍(lán)鳥(niǎo)生物因未能與德國(guó)政府達(dá)成價(jià)格協(xié)議,決定將基因療法Zynteglo暫時(shí)撤出德國(guó)市場(chǎng),此后公司漸漸退出歐洲市場(chǎng)。
對(duì)于Zynteglo在美國(guó)市場(chǎng)的定價(jià),F(xiàn)DA認(rèn)為,其價(jià)格在獨(dú)立審查小組認(rèn)為的具有成本效益的范圍。
據(jù)報(bào)道, 藍(lán)鳥(niǎo)生物在美國(guó)推出的付款模式是一次性預(yù)付款加上高達(dá)80%的風(fēng)險(xiǎn)分擔(dān)。如果患者在輸液后兩年內(nèi)未能保持免輸血,患者或保險(xiǎn)等商業(yè)機(jī)構(gòu)將獲得80%的費(fèi)用報(bào)銷。
藍(lán)鳥(niǎo)生物表示,美國(guó)大約有70%-75%依賴輸血的β-地中海貧血患者享受商業(yè)保險(xiǎn),公司正在與包括藥品福利管理機(jī)構(gòu)在內(nèi)的主要商業(yè)機(jī)構(gòu)進(jìn)行后期談判,同時(shí)也正在與一些州醫(yī)療補(bǔ)助機(jī)構(gòu)合作。
Zynteglo將在今年第四季度正式在美國(guó)上市,由于收集細(xì)胞到靜脈注射需耗時(shí)70~90天,預(yù)計(jì)正式治療將于2023年第一季度啟動(dòng)。

上世紀(jì)70年代,基因治療的概念首次提出。到90年代,美國(guó)基因治療的臨床試驗(yàn)如火如荼。1995年,美國(guó)出現(xiàn)了第一個(gè)基因治療成功的臨床案例,基因治療開(kāi)始備受矚目。
藍(lán)鳥(niǎo)生物就誕生于這個(gè)浪潮之中,1992年,麻省理工學(xué)院的兩名研究員創(chuàng)立了藍(lán)鳥(niǎo)生物的前身Genetix Pharmaceuticals。
在隨后的數(shù)十年內(nèi),基因技術(shù)發(fā)展逐漸成熟,生物技術(shù)公司也越來(lái)越得到資本市場(chǎng)的青睞。藍(lán)鳥(niǎo)生物乘勝追擊,2013年登陸納斯達(dá)克,上市前定價(jià)為每股17美元,上市當(dāng)日即上漲50%,接近每股26美元。到2018年時(shí),該公司股價(jià)沖上最高點(diǎn)——231美元/股,而彼時(shí),藍(lán)鳥(niǎo)生物還沒(méi)有產(chǎn)品正式上市。
直到2019年,藍(lán)鳥(niǎo)生物的基因療法Zynteglo在歐盟獲批有條件上市,但遭遇重大挫折后在2021年退出該地區(qū)。隨后,該公司另一款治療腦性腎上腺腦白質(zhì)營(yíng)養(yǎng)不良的基因療法Skysona也從歐洲市場(chǎng)撤離。
屋漏偏逢連夜雨。2020年5月,藍(lán)鳥(niǎo)生物與BMS聯(lián)合開(kāi)發(fā)的用于難治性多發(fā)性骨髓瘤患者的CAR-T療法bb2121,因數(shù)據(jù)不足被FDA延遲批準(zhǔn)。同年11月,藍(lán)鳥(niǎo)生物用于鐮刀狀細(xì)胞貧血癥(SCD)的基因療法LentiGlobin上市申請(qǐng)也被推遲一整年。
經(jīng)歷多番挫折后,藍(lán)鳥(niǎo)生物就開(kāi)始了下坡路,其股價(jià)也一路下行。截至美股周四收盤(pán),其股價(jià)較2018年的峰值暴跌97.5%。
記者查閱藍(lán)鳥(niǎo)生物近年財(cái)報(bào)發(fā)現(xiàn),2019年、2020年和2021年,該公司凈虧損分別達(dá)到7.9億美元、6.2億美元和8.2億美元。藍(lán)鳥(niǎo)生物2021年財(cái)報(bào)顯示,該公司僅擁有約4.42億美元的可用現(xiàn)金和相關(guān)流動(dòng)資產(chǎn)。
此番Zynteglo在美國(guó)的獲批或許有助于重振藍(lán)鳥(niǎo)生物的業(yè)務(wù)。彭博分析師Marc Engelsgjerd 在一份報(bào)告中寫(xiě)道,“在經(jīng)歷歐洲的失敗和美國(guó)監(jiān)管的延誤后,該許可(為藍(lán)鳥(niǎo)生物)提供了一條獲得可觀收入的途徑”。
根據(jù)藍(lán)鳥(niǎo)生物2021年的財(cái)報(bào),藍(lán)鳥(niǎo)生物的三款基因療法——Zynteglo、Skysona和LentiGlobin都將迎來(lái)新的里程碑,并有望為其帶來(lái)新的營(yíng)收增長(zhǎng)。目前,Zynteglo已經(jīng)向市場(chǎng)邁出了重要的一步。該公司認(rèn)為,Skysona也有望在2022年被批準(zhǔn)且獲得優(yōu)先審查,同時(shí)LentiGlobin有望明年第一季度提交許可證申請(qǐng)。?

中國(guó)企業(yè)也在開(kāi)發(fā)地貧基因療法
β-地中海貧血,在全世界流行,同樣,在中國(guó),地貧患者數(shù)量亦在增加。
2021年5月發(fā)表的《中國(guó)地中海貧血藍(lán)皮書(shū)(2020)》數(shù)據(jù)顯示,地貧基因攜帶者約占全球3.45億人口,而中國(guó)地貧基因攜帶者約有3000萬(wàn)人,重型和中間型地貧患者人數(shù)在30萬(wàn)左右,并且正以每年約10%的速度遞增。
由于血液資源有限和鐵螯合劑成本高昂,中國(guó)地貧患者僅有部分比例能維持規(guī)范輸血和規(guī)范去鐵治療,地貧患者的生存率明顯低于發(fā)達(dá)國(guó)家。
目前,中國(guó)的企業(yè)也正在開(kāi)發(fā)治療地貧基因療法。
據(jù)第一財(cái)經(jīng),今年8月16日,上海邦耀生物科技有限公司(以下簡(jiǎn)稱“邦耀生物”)宣布,其針對(duì)輸血依賴型β-地中海貧血的基因療法產(chǎn)品“BRL-101自體造血干祖細(xì)胞注射液”的臨床試驗(yàn)申請(qǐng),于當(dāng)天正式取得中國(guó)藥監(jiān)局藥品審評(píng)中心的批準(zhǔn)。
雖然邦耀生物的BRL-101與藍(lán)鳥(niǎo)生物的Zynteglo都屬于基因療法產(chǎn)品,但兩者仍有差別,前者屬于基因編輯療法產(chǎn)品,后者屬于慢病毒基因療法產(chǎn)品。
邦耀生物表示,當(dāng)前對(duì)于地貧傳統(tǒng)療法中,造血干細(xì)胞移植是唯一可以根治β-地中海貧血的方法,但費(fèi)用昂貴,且配型極其困難,僅有少部分患者能獲得移植,如果可以將自體造血干細(xì)胞經(jīng)基因校正后回輸?shù)交颊唧w內(nèi),則可以解決造血干細(xì)胞來(lái)源不足及配型困難的問(wèn)題,而CRISPR基因編輯技術(shù)的進(jìn)展給這種治療策略提供了可能。BRL-101是基于該公司自主研發(fā)的造血干細(xì)胞平臺(tái)開(kāi)發(fā)的基因治療產(chǎn)品,該平臺(tái)主要是利用基因編輯系統(tǒng)對(duì)患者的造血干細(xì)胞進(jìn)行基因修飾,修飾后的造血干細(xì)胞回輸?shù)交颊唧w內(nèi),通過(guò)自我更新和分化重建修飾細(xì)胞群體,從而達(dá)到治療血液系統(tǒng)疾病的目的。
邦耀生物亦表示,相比其它β-地貧基因療法動(dòng)輒上千萬(wàn),該公司的造血干細(xì)胞基因療法更為高效、便捷和安全,具有靶向性好、安全性高、作用范圍廣、治療效果顯著等優(yōu)勢(shì),可以做到一次治療終身治愈,并且成本可極大降低,有望成為更惠及大眾的療法。
在邦耀生物BRL-101宣布獲批臨床之前,2021年1月,博雅輯因針對(duì)輸血依賴型β地中海貧血的在研產(chǎn)品ET-01也在中國(guó)獲批開(kāi)展臨床試驗(yàn)。同樣,ET-01也屬于基因編輯療法產(chǎn)品。
記者| 文巧
編輯| 程鵬?蘭素英?易啟江
校對(duì)|段煉
封面圖片來(lái)源:視覺(jué)中國(guó)(圖文無(wú)關(guān))
部分綜合自第一財(cái)經(jīng)

|每日經(jīng)濟(jì)新聞 ?nbdnews??原創(chuàng)文章|
未經(jīng)許可禁止轉(zhuǎn)載、摘編、復(fù)制及鏡像等使用
如需轉(zhuǎn)載請(qǐng)與《每日經(jīng)濟(jì)新聞》報(bào)社聯(lián)系。
未經(jīng)《每日經(jīng)濟(jì)新聞》報(bào)社授權(quán),嚴(yán)禁轉(zhuǎn)載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請(qǐng)作者與本站聯(lián)系索取稿酬。如您不希望作品出現(xiàn)在本站,可聯(lián)系我們要求撤下您的作品。
歡迎關(guān)注每日經(jīng)濟(jì)新聞APP
